27Aug
みなさん、こんにちは。
ここ最近で急激に話題となっているリチウムイオンバッテリーに関する内容について、
何回かに分けて投稿していきたいと思います。
変更の可能性もありますが、
第1回 リチウムイオンバッテリーとは…
第2回 リチウムイオンバッテリーの種類と特性
第3回 リチウムイオンバッテリーの危険性とその対策
第4回 リチウムイオンバッテリー製品の処分
第5回 リチウムイオンバッテリー製品の普及と事故の増加
おおよそこの5回にわけていきたいと思います。
今日は初回なので、「リチウムイオンバッテリーというもの」について書いていきます。
リチウムイオンバッテリーは、
いわゆる二次電池に分類され、充電をすることによって繰り返し使用することが出来る電池です。
今現在のリチウムイオンバッテリーとしての開発が出来たのは1980年代のことです。
その頃までの二次電池は鉛バッテリーが多く用いられ、電子機器の小型化やそもそもの携帯機器の開発に伴い、
バッテリーも小型・大容量化が求められ、1970年代後半から開発が進められていました。
ニッケル水素電池の製品化もこの頃から始まりました。
さて、そんなリチウムイオンバッテリーですが、製品化され、世に広まったのは、1990年代に入ってからのことです。
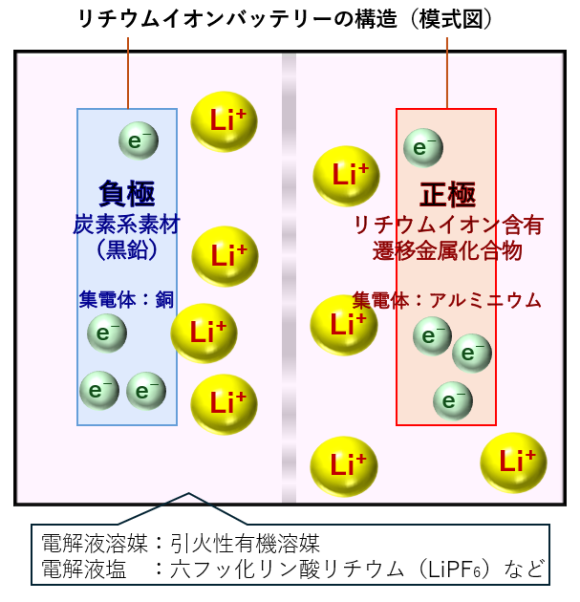
リチウムイオンバッテリーは、その名の通りリチウムイオンによって充放電が行われるバッテリーです。
正極(+極)にリチウム化合物を使用し、負極(-極)に黒鉛が用いられることが多く、
それぞれの電極はセパレータという小さな穴が開いたポリプロピレン(PP)やポリエチレン(PE)から作られた仕切りによって隔てられています。
バッテリー内部は電解液によって満たされ、
バッテリーの内部では、その電解液中をリチウムイオンが移動することで
バッテリーの外部からの電気エネルギーを化学エネルギーとして蓄えたり、蓄えた化学エネルギーを電気エネルギーとして用い、接続回路へ電気が流します。
リチウムイオンバッテリーの正極に用いる素材やそれによる性質の違いは、次回のブログでお話します。
ざっと上記の流れを模式図にしました。
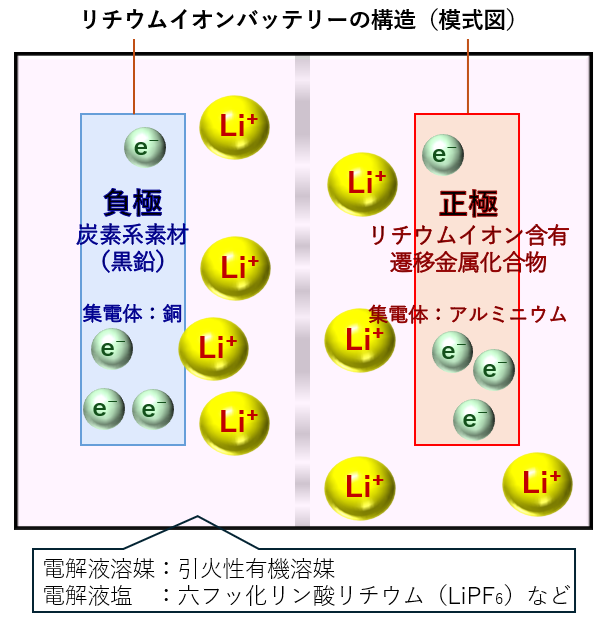
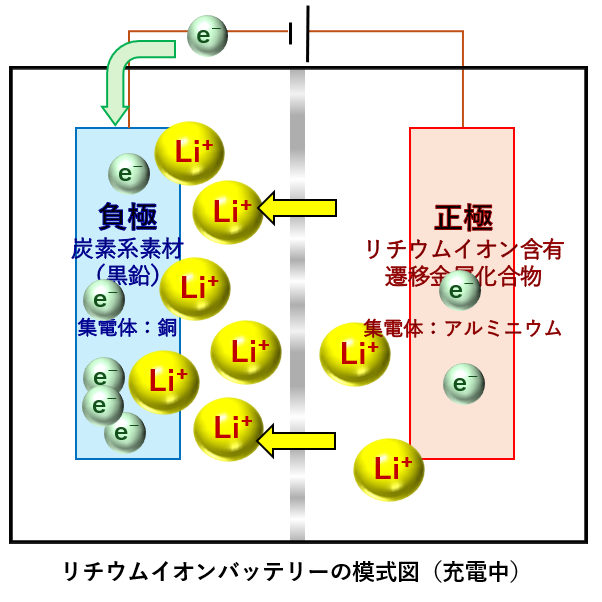
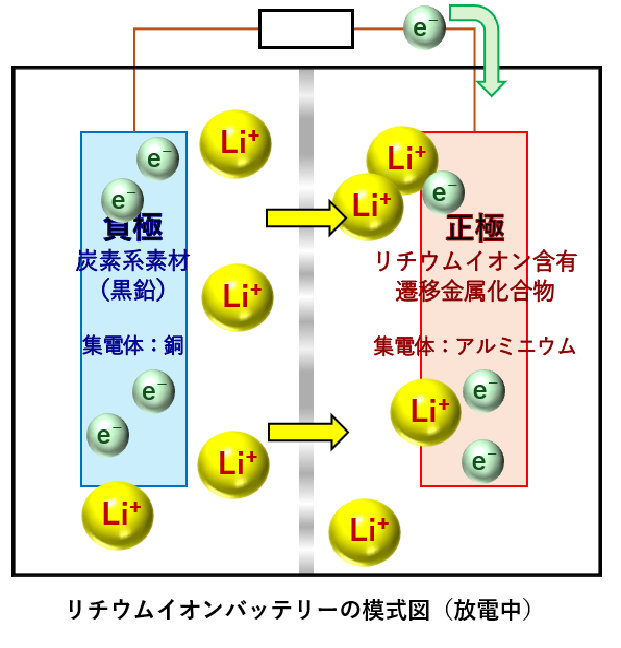
※電解液溶媒とは、電解液塩を溶解するための溶媒であり、これらで構成される電解液がイオンの移動を担っています。
後の回の予告として、この電解液溶媒として利用されている有機溶媒が発火事故の原因の1つであるということをお伝えしておきます。
さて、電極の材質による違いはあるものの、なぜリチウムイオンバッテリーはここまで世に広まったのでしょうか。その長所について考えてみましょう。
リチウムイオンバッテリーは二次電池の中でも近年になって開発が行われ、製品化がされました。現在実用化されている二次電池の中でエネルギー効率が高く、小型化・軽量化に大きく貢献することになりました。
リチウムイオンバッテリーの公称電圧は3.6~3.7V前後であり、他の電池よりも高い電圧を発揮でき、同一の電圧を求められる際に、より小型化・軽量化に貢献しています。
ちなみに、公称電圧はニッケル水素電池が約1.2V、鉛畜電池が約2.1V、身近な乾電池が1.5Vです。
それ以外にも自己放電が少ないことや充電/放電効率が高いのも大きなメリットです。
すべてのバッテリーと比較するとキリがありませんが、
このように非常にバランスが良く汎用性に富んだバッテリーであるために多くの場面で用いられるようになりました。
それでは、次回は「リチウムイオンバッテリーの種類と特性」についてお届けします。










